VIDA URBANA
Após Butantan, Fiocruz também pede autorização para uso emergencial de vacina contra Covid-19
Anvisa tem um prazo de 10 dias para analisar o pedido.
Publicado em 08/01/2021 às 16:09
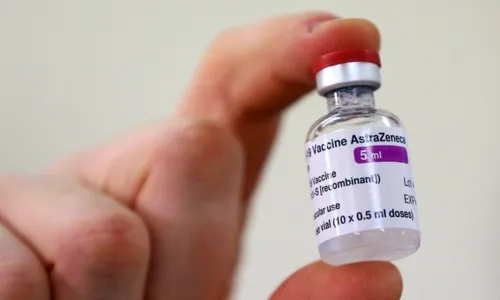
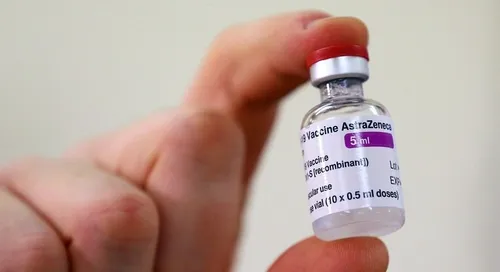
A Fiocruz entregou à Agência Nacional de Vigilância Sanitária (Anvisa) o pedido de uso emergencial da vacina contra a Covid-19 desenvolvida pelo laboratório AstraZeneca e pela Universidade de Oxford. O pedido feito nesta sexta-feira (4) é para 2 milhões de doses que devem ser importadas do laboratório Serum, sediado na Índia. Mais cedo, o Instituto Butantan pediu o uso emergencial da CoronoVac.
Segundo a Anvisa, o prazo para a análise do pedido de uso emergencial é de dez dias. Já a avaliação do pedido de registro definitivo é feita em até 60 dias.
Em meados de dezembro, a Diretoria Colegiada da Anvisa aprovou as regras para a autorização temporária de uso emergencial, em caráter experimental, de vacinas contra a Covid-19.
A concessão estabelecida pela Anvisa segue o modelo de autorizações emergenciais adotadas em outros países, como Reino Unido, Estados Unidos e Canadá, e vale apenas para o período de pandemia e até a vacina receber o registro definitivo.
Os principais pontos do uso emergencial das vacinas são seguintes:
- Cada pedido deve ser feito pela empresa desenvolvedora e será analisado de forma independente;
- Decisão será tomada pela Diretoria Colegiada da Anvisa;
- Serão considerados estudos não-clínicos e clínicos (em humanos);
- Serão itens avaliados: qualidade, boas práticas de fabricação, estratégias de monitoramento e controle, e resultados provisórios de ensaios clínicos;
- Empresa interessada deverá comprovar que a fabricação e a estabilidade do produto garantem a qualidade da vacina;
- Estudo clínico na fase 3 – última etapa de testes – deve estar em andamento e conduzido também no Brasil;
- Vacina com uso emergencial liberado não pode ser comercializada, ela só pode ser distribuída no sistema público de saúde;
- Liberação de uso emergencial pode ser revogada pela Anvisa a qualquer momento.

Comentários